Profesionales
PROTOCOLO DE LA INVESTIGACIÓN
Comisión Nacional de Bioética en Salud solicita suspender ensayo de vacuna china en Ecuador
Ecuador tiene hasta ahora la aprobación de uso de dos vacunas
Miércoles, 17 de febrero de 2021, a las 15:08
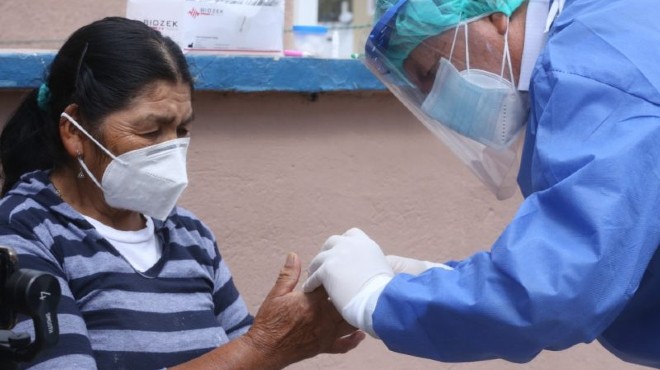
Estaba previsto realizar pruebas en Quito y Guayaquil. |
Redacción. Quito
Un documento al que tuvo acceso EDICIÓN MÉDICA ha señalado que la Comisión Nacional de Bioética en Salud solicitó suspender el ensayo clínico de una vacuna contra el SARS COV-2 con placebo como comparador, hasta esclarecer algunas dudas bioéticas en su realización.
Acceda aquí al documento completo
Si bien “existe el deber ético de hacer investigación” durante la pandemia de COVID19, ésta debe contar con las todas “garantías éticas”, y según esta comisión el ensayo de vacuna presentado por el laboratorio chino Anhui Zhifei Logcom “podría incumplir las normas éticas de investigación biomédica y la reglamentación nacional que la regula”.
En diciembre de 2020, el Ministerio de Salud Pública (MSP) anunció que el Ecuador se preparaba para participar en un proyecto de investigación clínica fase 3, de una nueva vacuna recombinante para la prevención de la COVID-19.
La vacuna desarrollada en colaboración con el Instituto de Microbiología de la Academia de Ciencias China (IMCAS) y su proceso de aprobación debe ser además revisado y autorizado por la Agencia de Regulación, Control y Vigilancia Sanitaria (ARCSA) y la Agencia de Aseguramiento de la Calidad de los Servicios de Salud y Medicina Prepagada (ACESS).
Según adelantó el MSP en diciembre, el estudio se encuentra registrado por la Organización Mundial de la Salud (OMS) y el Instituto Nacional de Higiene (INH) de Estados Unidos y buscaba ser aplicado en alrededor de 5 mil voluntarios en Ecuador.
No obstante, la misiva ha precisado que la propuesta “incumpliría las normas éticas universales señaladas en diversos instrumentos, entre ellos las Pautas Éticas internacionales para la Investigación y Experimentación Biomédica en Seres Humanos del Consejo de Organizaciones Internacionales de las Ciencias Médicas, (CIOMS), Organización Mundial de la Salud. (OMS), y la Declaración de Helsinki”.
En ese sentido, el Comité ha exhortado “al necesario cumplimiento” de esas normas y de “principios y valores fundamentales establecidos para estas circunstancias”.
Hasta el cierre de esta edición, la página web del MSP no ha emitido un pronunciamiento oficial respecto a la recomendación del Comité y mantiene su comunicado sobre el ensayo clínico (Enlace disponible aquí).
También lea: 8.000 ecuatorianos participarán en ensayo clínico fase 3 de una vacuna china contra la CoVID19