Salud Pública
PARA COVID-19
EMA respalda uso de la vacuna de Moderna en adolescentes de 12 a 17 años
En mayo, la farmacéutica afirmó que producto era seguro y eficaz en ese grupo de edad
Viernes, 23 de julio de 2021, a las 10:26
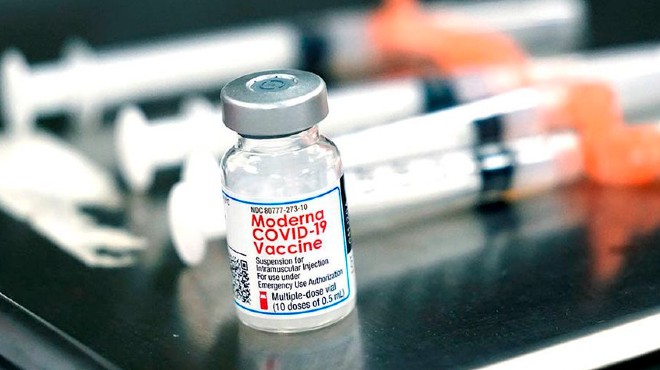
La farmacéutica nombró a su vacuna como Spikevax. |
Redacción. Quito
El Comité de Medicamentos Humanos (CHMP) de la Agencia Europea del Medicamento (EMA), ha recomendado el uso de la vacuna contra la COVID-19 de Moderna para jóvenes entre los 12 y los 17 años, allanando el camino para que se convierta en la segunda inyección autorizada para uso en adolescentes.
El uso de la denominada vacuna Spikevax de Moderna en ese grupo de edad será el mismo que en los mayores de 18 años con la administración de dos dosis, con cuatro semanas de diferencia.
El medicamento ha sido investigado en un estudio en el que participaron 3.732 niños de entre 12 y 17 años. La investigación continúa en curso y se está desarrollando de acuerdo con el Plan de Investigación Pediátrica (PIP) de Spikevax, acordado por el Comité Pediátrico de la EMA.
La inmunización ha producido una respuesta de anticuerpos comparable en los jóvenes de entre 12 y 17 años a la generada en los adultos con edades comprendidas entre los 18 y los 25 años. Ninguno de los 2.163 niños que recibieron la vacuna desarrolló COVID-19, en comparación con cuatro de los 1.073 que recibieron placebo. Estos resultados han permitido al CHMP concluir que la eficacia del suero en los jóvenes de entre 12 y 17 años es similar a la reportada por los adultos.
Según ha anticipado la farmacéutica creadora, los efectos secundarios más comunes incluyen dolor e hinchazón en el lugar de la inyección, dolor de cabeza, dolores musculares y articulares, agrandamiento de los ganglios linfáticos, escalofríos, náuseas, vómitos y fiebre. Estos efectos suelen ser leves o moderados y mejoran a los pocos días de la vacunación.
Pero el CHMP también ha señalado que, debido al número limitado de niños y adolescentes incluidos en el estudio, el ensayo no pudo haber detectado nuevos efectos secundarios poco frecuentes ni estimado el riesgo de efectos secundarios como miocarditis (inflamación del músculo cardíaco) y pericarditis (inflamación de la membrana que rodea el corazón).
Sin embargo, el comité ha considerado que los beneficios de la vacuna en esas edades superan los riesgos, y que la seguridad y eficacia continuará siendo monitorizada tanto en niños como en adultos mediante los datos de las campañas de vacunación de los Estados miembros a través del sistema de farmacovigilancia de la Unión Europea, los estudios en curso y las autoridades europeas.